Definición de Electronegatividad
En el fascinante mundo de la química, la electronegatividad se refiere a la tendencia intrínseca de los átomos dentro de una molécula para atraer electrones en un enlace covalente. Esta propiedad varía según el elemento y es crucial para comprender el comportamiento de las moléculas durante las reacciones químicas. Es interesante notar que, cuando dos átomos exhiben electronegatividades similares, comparten los electrones de manera más equitativa. En contraste, un átomo con una marcada propensión a atraer electrones será considerado de mayor electronegatividad.
La Relevancia de la Electronegatividad
La importancia de la electronegatividad es innegable en la química moderna. Su diferencia entre dos átomos puede ser un indicador predictivo de la reactividad química entre ellos. Un átomo con una elevada electronegatividad es capaz de atraer electrones cercanos, pudiendo incluso provocar la oxidación del otro átomo en la unión.
Propiedades Fundamentales de la Electronegatividad
La electronegatividad está influenciada por la estructura electrónica de los átomos, específicamente por cómo los electrones se distribuyen alrededor del núcleo y cómo el núcleo mismo ejerce su influencia sobre estos electrones. Los halógenos son un buen ejemplo de elementos con alta electronegatividad, manteniendo su nube electrónica densamente compactada a pesar de la repulsión que pueda existir entre los electrones. Para ilustrar, consideremos los átomos de potasio y cloro: el potasio alberga 19 electrones en un radio de 196 picómetros y presenta una electronegatividad de 0.445, mientras que el cloro contiene 17 electrones en un radio de solo 99.4 picómetros con una electronegatividad considerablemente más alta de 3.475. Además, los diferentes estados de oxidación pueden afectar la electronegatividad de un átomo, con estados de oxidación más altos generalmente asociados con electronegatividades menores.
| Elemento | Número de Electrones | Radio (picómetros) | Electronegatividad |
|---|---|---|---|
| Potasio (K) | 19 | 196 | 0.445 |
| Cloro (Cl) | 17 | 99.4 | 3.475 |
Variación de la Electronegatividad en la Tabla Periódica
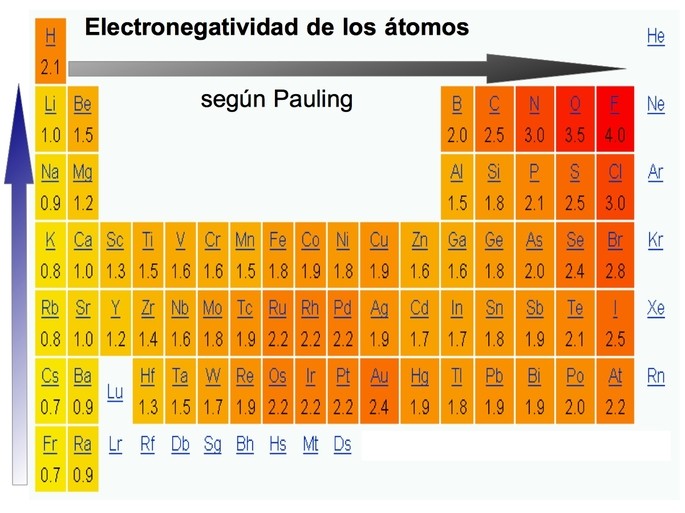
Observando la Tabla Periódica, es evidente que la electronegatividad crece progresivamente de izquierda a derecha a lo largo de un período y decrece de arriba hacia abajo en un grupo. Este patrón revela que, dentro del grupo de los metales alcalinos, el litio se destaca como el más electronegativo y el francio como el menos. Además, en el tercer periodo, el cloro ostenta la mayor electronegatividad frente al sodio que posee la menor.
Escala de Electronegatividad de Pauling
La electronegatividad, aunque no es directamente medible, puede inferirse a través de otros parámetros atómicos. Entre las diversas escalas disponibles, la formulada por Linus Pauling es la más reconocida y se ha actualizado recientemente. El método de Pauling estima la electronegatividad basándose en la energía de enlace del elemento en cuestión. Además, en 2018, se publicó una nueva tabla de electronegatividad elaborada por Martin Rahm, Tao Zeng y Roald Hoffmann, la cual incluye 96 nuevos valores para los elementos de la tabla periódica, calculados a partir de la energía promedio de enlace de los electrones de valencia. Estos valores se expresan en unidades de energía por electrón (eV e-1), siendo convertibles a la escala de Pauling a través de una relación de conversión establecida.
Relación entre Electronegatividad y Tipo de Enlace
La electronegatividad determina el tipo de enlace que se formará entre dos átomos. Por ejemplo, un par de átomos con una electronegatividad idéntica compartirán sus electrones de manera uniforme, resultando en un enlace covalente no polar. En contraste, una diferencia de electronegatividad entre 0.4 y 1.7 implica la formación de un enlace covalente polar. Finalmente, una diferencia mayor a 1.9 sugiere un enlace iónico, donde los electrones se transfieren del átomo menos electronegativo al más electronegativo, como se evidencia en el cloruro de sodio (NaCl).