Comprendiendo el Proceso Isométrico
Estimados lectores, soy Flavio, y hoy les traigo una explicación detallada sobre una operación fundamental en la termodinámica: el proceso isométrico, también denominado proceso isocórico o isovolumétrico. En este fenómeno particular, nos encontramos frente a una situación en la que el volumen permanece inalterado, es decir, no experimenta variación alguna a lo largo del tiempo considerado.
Durante un proceso isométrico que involucra un gas ideal, observamos una relación directamente proporcional entre la presión y la temperatura, correlación que es descrita precisamente por la ley de Charles. Sin embargo, es importante mencionar que dicha ley no aplica para gases reales, donde la interacción entre las moléculas y otros factores complejizan el comportamiento.
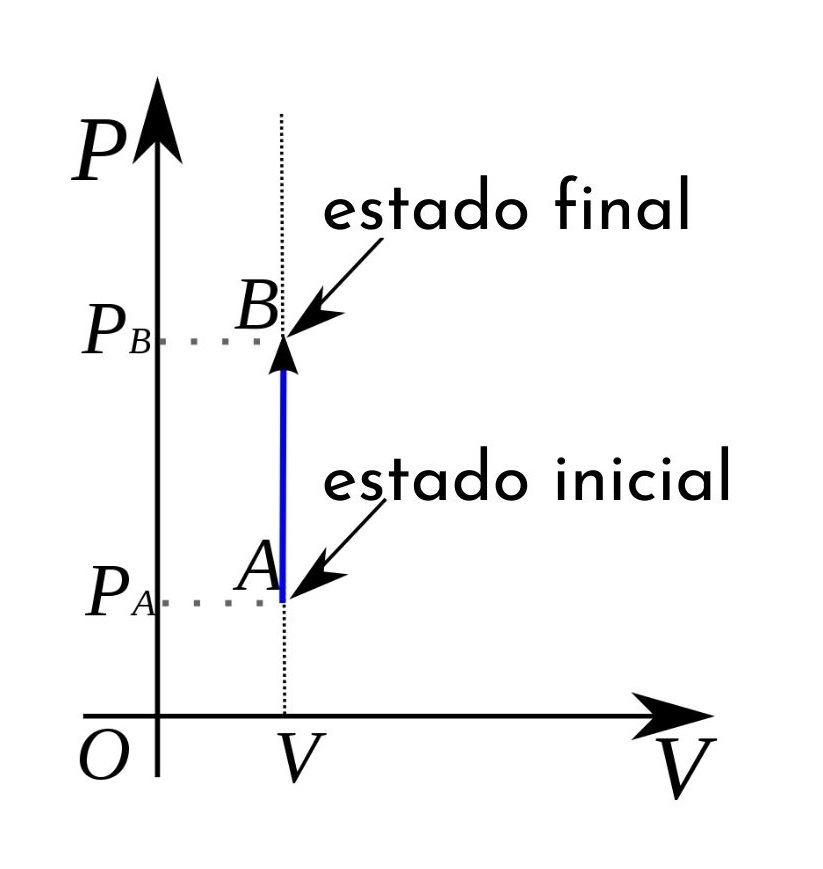
Cuando representamos gráficamente estos procesos, nos encontramos con las denominadas isocoras, que son líneas específicas en los diagramas que interrelacionan la temperatura (T), el volumen (V) y la presión (P). En el idealizado mundo de los gases perfectos, estas líneas se presentan como rectas.
Fórmulas Esenciales del Proceso Isométrico
Las ecuaciones matemáticas son herramientas vitales para desentrañar las propiedades de los procesos isométricos. Permiten, entre otras cosas, el cálculo de distintas variables y estados del sistema en estudio.
Cálculo del Trabajo
En el marco de un proceso isométrico, no se realiza trabajo ya que el volumen no cambia, es decir, ΔV es cero. Por ende, la fórmula para calcular el trabajo (W = P·ΔV) resulta en un producto de la presión (P) por cero.
Variación de la Energía Interna
Aplicando la primera ley de la termodinámica, llegamos a la de que la variación de la energía interna (ΔU) es igual a la diferencia entre el calor transferido al sistema (Q) y el trabajo realizado (W). En un proceso isométrico, como no hay trabajo, la variación de la energía interna se simplifica a ΔU = Q.
Calor Liberado
Cuando el número de moles de gas se mantiene constante, la variación de la energía es proporcional a la diferencia de temperatura (ΔT), lo cual se expresa a través de la fórmula Q=n·Cv·ΔT, donde Cv representa el calor específico molar a volumen constante y n es el número de moles del gas.
Ejemplos Prácticos de Procesos Isométricos
Para ilustrar mejor, consideremos el acto de calentar agua en una olla a presión: aquí el volumen se mantiene fijo. Esto contrasta con un proceso isobárico que tendría lugar si calentáramos agua en una olla común sin tapa. Además, en la industria automotriz, durante la combustión de la gasolina y la expulsión de gases en los motores, se presentan ejemplos claros de procesos isométricos. Un caso más en ingeniería mecánica es el ciclo de Stirling, caracterizado por sus etapas de calentamiento y enfriamiento a volumen constante.
| Concepto | Descripción |
|---|---|
| Proceso Isométrico | Proceso termodinámico donde el volumen permanece constante. |
| Relación Presión-Temperatura | Directamente proporcionales en gases ideales según la ley de Charles. |
| Isocoras | Líneas en diagramas P-V-T que representan procesos a volumen constante en gases ideales. |
| Trabajo en Proceso Isométrico | Nulo, debido a que no hay cambio de volumen (ΔV=0). |
| Var. de Energía Interna (ΔU) | En un proceso isométrico, ΔU = Q ya que W=0. |
| Calor Liberado (Q) | Depende del calor específico molar a volumen constante y la variación de temperatura. |
| Ejemplos | Olla a presión, motores de combustión, ciclo de Stirling. |